Avanços e novas perspectivas no manejo da migrânea
Lucas Resende Lucinda Mangia
Departamento de Otorrinolaringologia e Oftalmologia da Universidade Federal do Paraná (UFPR)
A migrânea é uma entidade clínica extremamente prevalente nas populações. Tem ganhado destaque crescente na Otoneurologia em decorrência dos avanços no entendimento de sua relação com o sistema vestibular. Seu reconhecimento é importante fator no surgimento de sintomas vestibulares recorrentes e sua presença marcante nos consultórios e ambulatórios da área – um provável reflexo do estilo de vida contemporâneo no mundo ocidental. A literatura médica em relação à migrânea ganhou exponencial robustez nas últimas décadas. Com ela, surgiram novas abordagens farmacológicas que têm modificado os planos terapêuticos ofertados aos pacientes, tanto durante a crise quanto como estratégias profiláticas. Sublinha-se que, apesar de promissoras para outros quadros relacionados à migrânea – como a migrânea vestibular, os ensaios clínicos que as validaram foram realizados no contexto centralizado na dor de cabeça para a seleção, inclusão e investigação dos resultados terapêuticos. Assim, sua extrapolação para outras situações é baseada no compartilhamento de fenômenos fisiopatológicos – sem lastro experimental suficiente até o momento.
Os desenvolvimentos mais significativos dos últimos anos no tratamento da migrânea exploram apresentações diversas da doença. Destarte, há alguns anos a toxina onabotulínica tem sido utilizada sobretudo para o tratamento preventivo de enxaqueca crônica em adultos no Brasil. Trata-se de uma neurotoxina derivada da bactéria Clostridium botulinum cujo efeito mais conhecido é a inibição da liberação de acetilcolina nas terminações nervosas periféricas, impedindo a contração muscular local. Sua indicação em quadros migranosos é baseada nos resultados satisfatórios de dois ensaios clínicos randomizados (PREEMPT 1 e 2). Acredita-se que, nesse caso, ela atue inibindo a liberação de neuropeptídeos associados com o surgimento da dor, como o CGRP, neurocinina A e a substância P, coibindo e revertendo processos de sensibilização central existentes na migrânea crônica. A eficácia, segurança e tolerabilidade da toxina onabotulínica A foram demonstradas em estudos posteriores e seus efeitos adversos são raros, transitórios e leves. São uma alternativa a ser considerada em casos refratários e/ou crônicos, porém ainda não são conhecidos quais fatores predizem melhor resultado de sua utilização. Estudos preliminares indicam possível benefício em casos refratários de migrânea vestibular. Efeitos esses, na conectividade de áreas de integração multissensorial em análises por ressonância magnética funcional.
Outras linhas de desenvolvimento em ampla expansão envolvem, de modo mais direto, o papel de neurotransmissores – mais especificamente a serotonina, e de moléculas biologicamente ativas, sobretudo o peptídeo relacionado ao gene da calcitonina (CGRP, da sigla em inglês). Vários estudos implicaram a serotonina na patogênese da migrânea. A maior parte dos neurônios presentes no núcleo dorsal do rafe (local de emergência do nervo trigêmeo), nos gânglios trigeminais e também nas terminações nervosas do V par, é serotoninérgica. Dos sete tipos de receptores da serotonina, os subtipos 5-HT1, 5-HT2 e 5-HT3 são aqueles mais implicados na cadeia de eventos relacionados à crise de migrânea. Sugere-se que os diferentes subtipos de receptores 5-HT possuem efeitos distintos na doença. Alguns poderiam estar envolvidos no desencadeamento dos episódios sintomáticos (por exemplo, 5-HT1C), enquanto outros podem preveni-los (por exemplo, 5-HT1D). Alguns autores advogam que o efeito vasoconstritor da serotonina também poderia repercutir na cadeia fisiopatológica da migrânea.
Há séculos atrás, as parteiras já utilizavam esporão-de-centeio para mitigar sangramentos uterinos pós-parto e, em 1918, a ergotamina foi isolada pela primeira vez por Arthur Stoll. Protótipo dos alcaloides do ergot, a ergotamina e seus derivados passaram a ser muito utilizados, em especial na Medicina Obstétrica. Na década de 1940, estudos sobre o centeio levaram à descoberta da serotonina, uma molécula com notável efeito vasotônico. Desde então, foi iniciada uma jornada em busca de uma substância que imitasse os efeitos dos alcaloides do ergot sem seus efeitos adversos. Na última década do século passado, o início da comercialização dos triptanos (p. ex, sumatriptano, naratriptano) trouxe a expectativa de um tratamento eficaz e mais seguro para as crises de migrânea. Os triptanos são agonistas da serotonina e se ligam fortemente a três subtipos de receptores: 5-HT1B, 5-HT1D e 5-HT1F. A atuação sobre 5-HT1D inibe a liberação de neuropeptídeos pelos aferentes trigeminais perivasculares. Por outro lado, sua alta afinidade sobre o receptor 5-HT1B, densamente encontrado no músculo liso dos vasos sanguíneos cerebrais, parece ser a principal responsável pelo efeito vasoconstritor desse grupo de substâncias. Contudo, é também esse mesmo efeito vasotônico que as tornam contraindicadas para populações de risco cardiovascular e/ou cerebrovascular. De modo geral, são consideradas medicações eficazes, porém de segunda linha para as crises agudas de migrânea de moderada a alta intensidade. Seu uso deve ser ponderado aos eventuais efeitos adversos vasculares.
Mais recentemente, foi desenvolvida uma nova classe farmacológica para o tratamento agudo da migrânea, os ditans, cujo principal princípio estudado é o lasmiditan. São compostos agonistas serotoninérgicos seletivos para 5-HT1F, subtipo de receptor extensamente distribuído pelo sistema nervoso central, porém com limitado efeito vasoconstritor e com esparsa presença nas coronárias. Sua ativação hiperpolariza as terminações nervosas trigeminais, levando à contenção do evento considerado central na fisiopatologia da migrânea: a ativação trigeminovascular. Pelo efeito restrito sobre 5-HT1B, parecem promissores como alternativas mais direcionadas e seguras aos triptanos.
O CGRP é um peptídeo de 37 aminoácidos descoberto em 1982. Sua relação com a migrânea foi progressivamente desvendada, de modo que se tornou alvo potencial de novas terapêuticas para a doença. O peptídeo se mostrou importante na patogênese da migrânea por seu papel na modulação da transmissão nociceptiva no sistema trigeminovascular. Acredita-se que esse neuropeptídeo atue nas terminações trigeminais amplificando o processo inflamatório local, além de apresentar efeitos vasodilatadores que também podem incorrer em crises da doença. Ressalta-se que, tal qual a serotonina, o CGRP também é expresso no sistema vestibular e pode estar igualmente implicado na gênese da migrânea vestibular.
Os primeiros bloqueadores do receptor do CGRP, chamados gepants, demonstraram excelentes resultados no controle da crise, porém com riscos de lesão hepática. Avanços posteriores culminaram na aprovação de fármacos da classe para uso preventivo, o atogepant, e para o abortamento dos episódios sintomáticos, o rimegepant e o ubrogepant. O rimegepant, entretanto, tem se mostrado promissor também em seu uso profilático. Com isso, tais medicações podem futuramente tornar as fronteiras entre tratamentos de crise e profiláticos mais imprecisas. Atualmente, considera-se o uso abortivo dos gepants uma opção em pacientes com resposta insuficiente ou contraindicação aos triptanos.
Anticorpos monoclonais (mABs) injetáveis contra o receptor ou a molécula de CGRP também foram desenvolvidos e se mostraram capazes de prevenir a vasodilatação neurogênica no sistema nervoso central, sem alterar parâmetros fisiológicos cardiovasculares. É interessante notar que seus efeitos ocorrem apesar do fato de não atravessarem a barreira hematoencefálica. O erenumabe é o principal integrante dos mAbs direcionados ao receptor do CGRP. É usado mensalmente como injeção subcutânea e apresenta risco potencial de hipertensão arterial sistêmica. Foi descontinuado no Brasil por razões comerciais. O fremanezumabe e o galcanezumabe são mAbs direcionados ao CGRP de uso subcutâneo. Enquanto o fremanezumabe pode ser usado a cada três meses, o galcanezumabe deve ser usado mensalmente. O eptinezumabe é um mAbs também direcionado ao CGRP, mas de uso intravenoso trimestral. Foi demonstrada sua eficácia tanto em profilaxia quanto como medicação abortiva, porém não se encontra disponível em nosso país. Embora apresentem efeito moderado de resposta e ainda haja uma fração considerável de pacientes refratários, os mAbs se revelaram uma opção interessante para pacientes sem resposta com outras classes de medicação profilática. Teoricamente, ainda devem ser evitados naqueles com eventos isquêmicos recentes devido aos efeitos cardioprotetores e vasodilatadores do CGRP. Em comparação às outras classes, no entanto, aparentam ter baixa taxa de eventos adversos, baixo risco e comodidade posológica que pode facilitar a adesão terapêutica. Seu uso combinado a outras terapias foi pouco explorado até o momento. A FIGURA 1 ilustra esquematicamente os alvos moleculares de novas terapêuticas para migrânea que exploram a participação do CGRP e da serotonina em sua fisiopatologia.
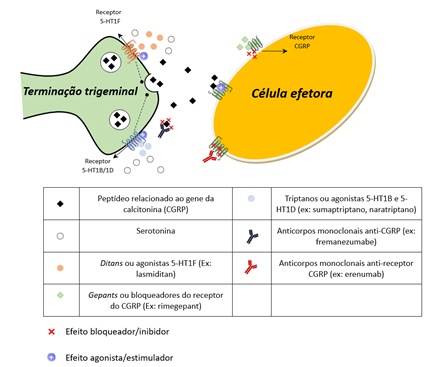
Figura 1: Alvos celulares e moleculares dos fármacos para migrânea que atuam nas vias fisiopatológicas envolvendo a serotonina e o CGRP.
Linhas de pesquisa ainda mais incipientes têm evoluído com a promessa de trazer novas alternativas farmacológicas ao controle da migrânea. Entre elas, pode-se citar o bloqueio da via do PACAP-38 (peptídeo ativador da adenilato ciclase pituitária). Trata-se de um neuropeptídeo que, à semelhança do CGRP, é liberado em crises migranosas e cujo receptor, denominado PAC1, é largamente encontrado no sistema trigeminovascular. Acredita-se que o PACAP-38 é capaz de modular a nocicepção em diferentes níveis do sistema nervoso central. O antagonismo do PAC1, por sua vez, reduz a sensibilidade à dor e parece ser um bom alvo terapêutico na migrânea. Nesse sentido, mAbs direcionados ao PAC1 têm sido desenvolvidos e novos estudos podem reforçar futuramente o arsenal terapêutico da migrânea.
Independentemente do olhar esperançoso para o futuro e as novas medidas farmacológicas em desenvolvimento, é essencial que o paciente com migrânea continue a ser avaliado e abordado de maneira abrangente, empática e personalizada. Como seu processo fisiopatológico é complexo e dinâmico, dificilmente haverá um fármaco único e milagroso para todos os pacientes. Dessa maneira, na mesma medida em que os médicos devem estar atentos às novidades, evidências científicas prévias merecem ser revisitadas. As possibilidades terapêuticas não-farmacológicas precisam ser sempre ponderadas e, idealmente, o manejo integral do indivíduo acometido deve continuar a embasar qualquer plano de tratamento proposto.
Referências:
- Ahn S, Balaban C. Distribution of 5-HT1B and 5-HT1D receptors in the inner ear. Brain Res. 2010;1346:92-101.
- Arkless K, Argunhan F, Brain SD. CGRP Discovery and Timeline. Handb Exp Pharmacol. 2019;255:1-12.
- Berman NEJ, Puri V, Chandrala S et al. Serotonin in trigeminal ganglia of female rodents: relevance to menstrual migraine. Headache 2006; 46: 1230–1234.
- Bordini CA, Roesler C, Carvalho D de S, et al. Recommendations for the treatment of migraine attacks – a Brazilian consensus. Arq Neuropsiquiatr. 2016 Mar;74(3):262-71.
- Brewerton TD, Murphy DL, Meuller EA et al. Induction of migraine-like headaches by the serotonin agonist, m-chlorophenylpiperazine. Clin Pharmacol Ther 1988; 43: 605–608.
- Dodick DW, Turkel CC, DeGryse RE, et al. OnabotulinumtoxinA for treatment of chronic migraine: pooled results from the double-blind, randomized, placebo-controlled phases of the PREEMPT clinical program. Headache. 2010 Jun;50(6):921-36.
- Durham P. Calcitonin gene-related peptide (CGRP) and migraine. Headache. 2006;46:S3-S8.
- Edvinsson L. CGRP and migraine: from bench to bedside. Rev Neurol (Paris). 2021 Sep;177(7):785-790. Iyengar S, Johnson KW, Ossipov MH, Aurora SK. CGRP and the Trigeminal System in Migraine. Headache. 2019 May;59(5):659-681.
- Escher CM, Paracka L, Dressler D, Kollewe K. Botulinum toxin in the management of chronic migraine: clinical evidence and experience. Ther Adv Neurol Disord. 2017 Feb;10(2):127-135.
- Fernández-Bravo-Rodrigo J, Pascual-Morena C, et al. The Safety and Efficacy of Calcitonin Gene-Related Peptide (CGRP) Monoclonal Antibodies for the Preventive Treatment of Migraine: A Protocol for Multiple-Treatment Systematic Review and Meta-Analysis. Int J Environ Res Public Health. 2022 Feb 3;19(3):1753.
- Ferrari MD, Melamed E, Gawel MJ, Treatment of migraine attacks with sumatriptan. N Engl J Med 1991; 325: 316–318.
- Grimsrud KW, Halker Singh RB. Emerging Treatments in Episodic Migraine. Curr Pain Headache Rep. 2018 Jul 16;22(9):61.
- Herd CP, Tomlinson CL, Rick C, Scotton WJ, Edwards J, Ives N, Clarke CE, Sinclair A. Botulinum toxins for the prevention of migraine in adults. Cochrane Database Syst Rev. 2018 Jun 25;6(6):CD011616.
- Koo JW, Balaban CD. Serotonin-induced plasma extravasation in the murine inner ear: Possible mechanism of migraine-associated inner ear dysfunction. Cephalalgia. 2006;26(11):1310-1319.
- Kowacs F, Roesler CAP, Piovesan EJ, et al. Consensus of the Brazilian Headache Society on the treatment of chronic migraine. Arq Neuropsiquiatr. 2019 Jul 29;77(7):509-520.
- Moreno-Ajona D, Chan C, Villar-Martínez MD, et al. Targeting CGRP and 5-HT1F Receptors for the Acute Therapy of Migraine: A Literature Review. Headache. 2019 Jul;59 Suppl 2:3-19.
- Oh SY, Kang JJ, Kim S, Lee JM, Kim JS, Dieterich M. A preliminary trial of botulinum toxin type A in patients with vestibular migraine: A longitudinal fMRI study. Front Neurol. 2022 Jul 25;13:955158.
- Pietrobon D, Moskowitz M. Pathophysiology of migraine. Annu Rev Physiol. 2013;75:365-391.
- Piovesan E, Cadecaro P, Pepe C. Análise de custo-efetividade da toxina onabotulínica A no tratamento preventivo da migrânea crônica sob a perspectiva do sistema privado de saúde do Brasil. Jornal Brasileiro de Economia da Saúde, v. 9, n. Suppl1, p. 71–80, 2017.
- Ray JC, Hutton EJ, Matharu M. OnabotulinumtoxinA in Migraine: A Review of the Literature and Factors Associated with Efficacy. J Clin Med. 2021 Jun 29;10(13):2898.
- Schytz H, Olesen J, Ashina M. The PACAP receptor: a novel target for migraine treatment. Neurotherapeutics. 2010;7(2):191-196.
- Taylor B K and Basbaum A I. Neurochemical characterization of extracellular serotonin in the rostral ventromedial medulla and its modulation by noxious stimuli. J Neurochem 1995; 65(2): 578–589.
- Vila-Pueyo M. Targeted 5-HT1F Therapies for Migraine. Neurotherapeutics. 2018 Apr;15(2):291-303.
- Wannmacher L, Ferreira MBC. Enxaqueca: mal antigo com roupagem nova. Uso racional de medicamentos: temas selecionados. Brasília: OPAS; 2004.


